 6
6 3
3 4
4 .5
.5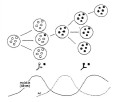 6
6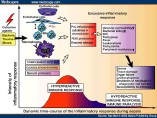 7
7 8
8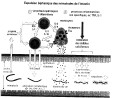 ,
, | accueil | immun1-19: Immunité anti-bactérienne, antivirale et anti-parasitaire : mécanismes effecteurs et échappement |
<-- cours --> |
objectifs pédagogiques (*) |
|
|
- décrire les principaux mécanismes effecteurs efficaces contre une bactérie (à habitat intra-cellulaire ou extra-cellulaire) ou un virus | |
définitions générales - messages |
|
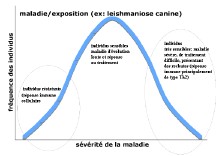
| mécanismes effecteurs/ mécanismes protecteurs | = ensemble des mécanismes de l'immunité ayant des effets biologiques efficaces dans une situation donnée (infection bactérienne..). L'immunité se décompose en nombreuses composantes, telles que la production d'anticorps neutralisants, l'activité NK.. Chacun des mécanismes de l'immunité est plus ou moins efficace selon les agents pathogènes en cause, en particulier selon leur localisation intra ou extracellulaire, ou leur sensibilité aux différentes molécules cytotoxiques (tableau1: principaux mécanismes antibactériens et antiviraux). Ainsi, on distinguera des mécanismes anti-bactériens, anti-viraux, anti-parasitaires, anti-tumoraux. La recherche a identifié pour un certain nombre de maladies les mécanismes qui sont les plus impliqués dans la protection, et les antigènes microbiens/parasitaires qui les induisent: la guérison surviendra d'autant plus rapidemment que l'individu sera capable de mettre en place ces mécanismes protecteurs en montant une immunité de qualité contre ces antigènes. Le polymorphisme individuel de l'immunité explique que pour chaque infection on trouvera au sein d'une espèce des individus plus ou moins sensibles ou résistants, en dehors du fait que l’exposition individuelle réelle à l’agent pathogène est variable. En effet, chaque individu est plus ou moins capable de produire la réponse immune appropriée, selon 3 facteurs principaux : - la qualité globale de la réponse immune (selon l’âge, l’état général..) - la capacité à reconnaître efficacement les antigènes impliqués dans la protection (selon les capacités de présentation par le CMH de l’individu) - la régulation qualitative de la réponse vers des mécanismes ± protecteurs, par exemple de type humoral ou cellulaire, selon les conditions de présentation des antigènes et les coopérations cellulaires mises en place.(fig1: polymorphisme de la résistance aux infections); fig2: diversité des mécanismes protecteurs selon le µorganisme Au contraire, des individus consanguins peuvent présenter une réponse homogène, protectrice ou non, vis-à-vis d’une infection donnée (cas des souris de laboratoire, mais aussi des élevages intensifs porcins ou volailles qui sont constitués de souches assez consanguines) fig3: exemples de variations de la protection en fonction du fonds génétique (exemple : résistance à la salmonellose de souris d’haplotype CMH b ou d, homozygote ou hétérozygote) fig4: schéma de l’ensemble des mécanismes antiviraux qui interviennent au cours d’une infection (Des mécanismes immuns non spécifiques puis spécifiques se succèdent. L’efficacité relative, ainsi que la cinétique d’induction, des anticorps et des lymphocytes cytotoxiques varie selon le type de virus) |
| échappement à la réponse immune | Quelques espèces et souches de µorganismes et parasites pathogènes sont capables de résister aux mécanismes de la défense immune et provoquent ainsi des maladies plus sévères ou plus durables que la moyenne. Dans une même genre bactérien ou viral, les espèces et les souches les plus pathogènes sont souvent celles qui présentent des capacités d'échappement (formes capsulées...). |
| participation de la réponse immune aux symptômes | Lors d'une infection/parasitose, les symptômes peuvent avoir une double origine: - directement liée au pouvoir pathogène de l'agent infectieux: multiplication microbienne (± atteinte des cellules infectées), production de toxines et enzymes (neurotoxine: paralysie..) - fonction de l'intensité des mécanismes effecteurs de l'immunité ("dommages collatéraux"). Plus les mécanismes effecteurs sont ciblés et efficaces contre l'agent infectieux, moins il y a de symptômes dus à l'inflammation et aux mécanismes non spécifiques (guérison rapide et symptômes bénins chez un individu immun). - symptômes liés aux mécanismes de défense non spécifique des tissus: toux, diarrhée, prurit.. - symptômes et lésions liés à la production de cytokines par les tissus atteints (facteurs chimiotactiques, cytokines pyrogènes, médiateurs de l'inflammation) et à l'activation du complément: fièvre (hyperthermie et troubles neuro-végétatifs), inflammation (oedème, infiltration cellulaire..). La production massive de cytokines en réponse à des endotoxines bactériennes peut-être à l'origine du "choc septique". - symptômes et lésions liés à la destruction des cellules infectées (activité CTL ..): la capacité de reconstitution d'un tissu est très variable selon son type (épithélium, musculaire, nerveux) et selon l'étendue de la destruction tissulaire. Les mécanismes de réparation peuvent dysfonctionner, entrainant des séquelles à long terme (fibrose..). Les symptômes seront directement fonction du tissu atteint (hépatite, pancréatite, myosite..). - complications liés aux réactions d'hypersensibilité (production excessive de complexes immuns...). |
| choc septique | Le choc septique est une atteinte brutale et sévère de l'organisme (défaillance cardio-vasculaire et insuffisance des principales fonctions), souvent mortelle. Elle est due à une production excessive de cytokines et de facteurs de l'inflammation en réponse à une infection, le plus souvent par des bactéries gram- (fig6: mécanismes immuns et inflammatoires au cours du choc septique). Le choc peut survenir au cours d'une infection massive chez un individu fragile (bactériémie/septicémie..), ou lors d'infections par des bactéries possédant des endotoxines et/ou super-antigènes connus pour leur virulence (streptocoques du groupe A, entérobactéries, Neisseria..). La principale cytokine impliquée dans le choc septique est le TNF, dont différentes formes sont produites par les tissus agressés et les lymphocytes T. A faible dose, le TNF est un activateur efficace de l'immunité, mais à forte dose -comme durant le chox septique-, le TNF est responsable d'inflammation, de troubles métaboliques et de destruction tissulaire. |
| immunité concomitante | immunité partielle d'un individu vis-à-vis d'une parasitose, aboutissant à un équilibre hôte-parasite où le parasite devient peu pathogène mais n'est pas éliminé; Le maintien de l'infestation est du à l'échappement des formes adultes ou à la persistance de formes parasitaires localisées dans des tissus peu accessibles à la réponse immune (kystes formés par des parasites quiescents dans le cerveau : toxoplasmose...). Cette immunité est spécifique (l'installation d'une immunité concomitante contre une espèce parasitaire ne modifie pas la sensibilité à d'autres parasites). Généralement, l'immunité concomitante diminue la multiplication/reproduction des parasites sans la bloquer totalement, et empêche la sur-infestation (destruction des stades infestants: larves..). Ainsi la symptomatologie et la ponte des œufs/larves/ookystes peut diminuer ou « onduler » au cours d’une infestation parasitaire alors que la charge en parasites adultes reste constante. L'immunité concomitante est lente à s'installer, et ne s'observe en fait que chez des individus adultes, expliquant pourquoi les jeunes sont bien plus sensibles aux infestations parasitaires. Malheureusement, cette immunité partielle disparait rapidement (en quelques semaines) après la mort des adultes: l'individu recevant un traitement anti-parasitaire redevient de ce fait sensible à une nouvelle infestation. Cette immunité peut diminuer lors de la gestation, expliquant "le réveil" des parasites et la transmission aux jeunes. fig7: augmentation de la production de larves de Toxocara lors de la lactation chez la chienne L'immunité concomitante est un phénomène fréquemment observé au cours des parasitoses (en particulier par des helminthes digestifs ou systémiques). Elle existe également pour certaines infections bactériennes chroniques. |
| rôle des IgE et des éosinophiles dans l'immunité anti-métazoaire | Les IgE et les éosinophiles sont particulièrement efficaces contre les parasites métazoaires (helminthes, acariens, puces..) car ils agissent en synergie sur de nombreux mécanismes: - les mastocytes et les éosinophiles sont présents en quantité abondante dans les tissus les plus souvent parasités (peau, paroi digestive..). - la concentration des IgE est maximale dans ces mêmes tissus (car elles se fixent préférentiellement sur les mastocytes et les éosinophiles). - les mastocytes, les basophiles et les éosinophiles sont très impliqués dans l'inflammation locale ainsi que dans l'activation des défenses locales (libération d'histamine par dégranulation: modification de la motricité et de la sécrétion muqueuse..): ces mécanismes s'exercent au dépend des parasites (diarrhée, toux, prurit, modification vasculaire, afflux de leucocytes..). Ces mécanismes sont principalement induits par les IgE et par des "signaux de danger" produits en cas de lésion tissulaire. - les éosinophiles sont capables de mécanismes cytotoxiques importants, principalement par dégranulation (mécanisme d'ADCC= Antibody dependent cell cytotoxicity): les molécules toxiques libérées attaquent la surface des parasites (destruction du revêtement parasitaire, en particulier au niveau des zones d'échange comme l'appareil buccal ou génital). Ces mécanismes sont principalement induits par les IgE. Fig8: principaux mécanismes immuns dirigés contre les helminthes intestinaux Toutefois ces réponses sont longues à s’installer (peu chez le jeune) et l'inflammation peut être importante lors de fortes infestations (diarrhées, prurit..). Dans certains cas de parasitoses digestives, on aboutit à un phénomène de « self-cure » où la réponse immune et inflammatoire est suffisamment efficace pour éliminer tous les parasites (après un ou plusieurs cycles de ponte tout de même !). |
| cas des protozooses | Les protozoaires sont des µorganismes bien plus sophistiqués que les bactéries, capables de s'adapter à différentes conditions de vie durant le cycle parasitaire. L'immunité doit de construire efficacement vis-à-vis de chaque stade du parasite, impliquant plusieurs mécanismes immuns, ce qui peut devenir extrêmement complexe: c'est pourquoi de nombreuses protozooses évoluent sur un mode chronique, et que la guérison complète est rare. - les protozoaires qui évoluent dans la lumière intestinale (coccidies, amibes..) induisent une immunité locale (IgAs agglutinantes.). Les cytokines produites localement provoquent de l’inflammation, peuvent bloquer l’invasion cellulaire et faciliter la phagocytose. - la protection contre les parasites intra-erythrocytaires dépend essentiellement de l'immunité humorale (d'où des complications possibles en cas de surproduction d'anticorps). Selon les parasites, les anticorps neutralisants, agglutinants et/ou opsonisants assurent la protection. - la protection contre les parasites intra-macrophagiques dépend essentiellement de l'immunité cellulaire: les parasites n'arrivent plus à former une vacuole parasitophore ou à sortir d'une vacuole de phagocytose lorsque le macrophage est activé par l'interferon gamma. |
| Les protozoaires développent de nombreux systèmes d'échappement et leurs antigènes sont souvent peu immunogènes: le plus souvent, l'individu développe un grand nombre de mécanismes immunitaires dont seule une petite partie est réellement protectrice (d’où la difficulté à développer des vaccins efficaces). Dans une population infestée, on observe souvent une distinction nette entre une population résistante et une population très sensible (qui développe une forme sévère): cela s'explique à la fois par le polymorphisme de l'immunité (± grande aptitude à reconnaitre les antigènes impliqués dans la protection selon le CMH de l'individu..), mais aussi par le très grand nombre de facteurs régulateurs qui interviennent dans le développement de la fraction protectrice de l'immunité (ex: les chiens présentant une forme grave de leishmaniose produisent beaucoup d'anticorps mais très peu d'interferon gamma). |
|
| cas des fungi | Peu de fungi sont parasites, et la plupart ne sont pathogènes lors de primo-infestation et sur un terrain fragilisé (individus immunodéprimés, manque d'hygiène, utilisation abusive d'antibiotiques..): teignes des jeunes.. Beaucoup d'infections fungiques de la peau et des muqueuses sont fortement inflammatoires (teignes, otite à Malassezia..), et se résolvent lentement en l'absence de traitement anti-fongique. |
| Participation de la réponse immune aux symptômes | ans les infections, les parasitoses, les tumeurs et toutes les maladies du système immunitaire, des mécanismes s'enclenchent pour rejetter l'agression. Il y a donc forcément des mécanismes tissulaires non spécifiques (toux, prurit..), de l'inflammation, des atteintes organiques liées aux mécanismes cytotoxiques. La réponse immune participe donc à l'expression clinique, surtout au début de l'agression. Lorsque l'infection/parasitose est contrôlée - mais pas complètement éliminée- par une réponse immune protectrice, les mécanismes non spécifiques et l'inflammation sont minimes, et donc les signes cliniques peuvent disparaitre quasiment : c'est le cas du "portage sain". Ce phénomène intervient très souvent dans les parasitoses, et aussi dans certaines infections microbiennes. Lors d'échappement à la réponse immune, les effets néfastes de la réponse immune peuvent expliquer les symptômes observés (fièvres ondulantes..). Cette physiopathologie liée à la réponse immune est très importante à comprendre dans le déroulement des maladies et dans leur traitement (utilisation raisonnée des anti-inflammatoires..). |
schémas et figures |
|
tableaux |
tableau 1: principaux mécanismes effecteurs anti-microbiens (fig6: exemples) |
bactéries extra-cellulaires |
bactéries intra-cellulaires |
virus |
|||
| immunité non spécifique | barrières immunes permanentes non spécifiques (pH, protéines anti-microbiennes: lysozyme..) | effet bactériostatique-bactéricide et virostatique-virucide, mais l'efficacité de chaque mécanisme est variable selon les µorganismes (lysozyme: destruction de la paroi gram+..) |
||||
| fièvre et inflammation | effet bactériostatique et virostatique plus ou moins important selon les µorganismes réduction de la dissémination du µorganisme dans l'organisme |
|||||
| interférons de type 1 (IFNalpha et IFNbeta) | peu d'effet |
peu d'effet |
diminue l'infectivité et empêche la dissémination virale dans un tissu (effet temporaire) |
|||
| système du complément (voie alterne ou classique: IgM>IgG) | cytolyse bactérienne (si gram-) opsonisation-phagocytose |
peu d'effet |
peu ou pas d' effet |
|||
| immunité humorale (dépend surtout d'une régulation de type Th2) | ||||||
| anticorps précipitants ou agglutinants (IgM et IgG) | élimination des antigènes solubles issus de la sécrétion bactérienne, ou des particules/antigènes solubles issus de la destruction microbienne (par les autres mécanismes immuns) |
|||||
| anticorps neutralisants (IgG) | neutralisation des facteurs de virulence: toxines, enzymes, facteurs d'adhésion.. (selon µorganisme) |
peu d'effet |
neutralisation des facteurs de penetration virale intracellulaire |
|||
| phagocytose par les neutrophiles (en présence d'anticorps opsonisants IgG ou IgA) | efficace (sauf germes échappant à la phagocytose: pus) |
peu d'effet |
pas d'effet |
|||
| autres mécanismes dépendant des anticorps (IgAs des muqueuses..) | exclusion immune (limite la contamination par voie muqueuse) régulation spécifique des mécanismes inflammatoires (dégranulation des mastocytes..) |
|||||
| activité des mastocytes et des éosinophiles (avec anticorps IgG ou IgE, ou avec anaphylatoxines..) | pas ou peu d'effet (mais participe à l'inflammation, en particulier dans les infections des muqueuses) |
|||||
| phagocytose par les macrophages (en présence ou non d'anticorps) | efficace en présence d'anticorps |
efficace si les bactéries ont pour cible les macrophages et que ceux-ci sont activés par l'IFNgamma |
pas d'effet |
|||
| immunité cellulaire (dépend surtout d'une régulation de type Th1 et de la production d'IFNgamma) | ||||||
| activité cytotoxique lymphocytaire CTL | pas d'effet |
destruction des cellules infectées (cas général) |
||||
| activité cytotoxique NK | pas d'effet |
destruction des cellules infectées (cas particulier: infections diminuant l'expression cellulaire du CMH) |
||||
tableau 2: exemples de mécanismes d'échappement des µorganismes et parasites |
exemple | conséquence | |
| 1- limiter la reconnaissance spécifique | exposer en surface des antigènes peu immunogènes (non protéiques..) | bactéries gram+, parasites | réponse spécifique faible et peu durable |
| produire des antigènes présentant une grande variabilité | HIV, paludisme.. | inefficacité des lymphocytes et des anticorps | |
| libérer des antigènes solubles | filaires, schistosomes.. | inutilité, voire nocivité, des anticorps | |
| 2- se cacher dans des zones peu accessibles à la réponse immune (formes intra-cérébrales, intra-oculaires..), souvent sous des formes peu actives | toxoplasmose, filariose.. | infections persistantes, avec rechute en cas de baisse de l'immunité | |
| 3- résister pied-à-pied aux mécanismes effecteurs | se protéger dans une capsule empêchant la phagocytose | bactéries pyogènes (streptocoques..) | infections suppurées |
| produire des enzymes détruisant les produits cytotoxiques des lysosomes | parasites et bactéries intracellulaires | infections persistantes: résistance à la lyse par les macrophages | |
| sortir de la vacuole de phagocytose vers le cytoplasme | |||
| produire des lymphotoxines et/ou cytotoxines détruisant les neutrophiles et/ou les lymphocytes | nombreux virus et bactéries | résistance à la phagocytose et à l'activité CTL, immunodepression | |
| 4- désorganiser la réponse immune | exposer et libérer des endotoxines | bactéries gram- | forte fièvre et inflammation (pouvant aller jusqu'au choc septique) |
| produire des superantigènes (de différents types) | quelques µorganismes et parasites | activation lymphocytaire anarchique (d'où inflammation++), ou au contraire destruction/inhibition des lymphocytes | |
| 5- autres! | nombreux autres, dont : |
virus, bactéries et parasites transmis par des arthropodes | nombreux mécanismes favorisant l'invasion : agents inhibiteurs de l'inflammation ou enzymes cytolytiques contenues dans la salive! |
élements d'application et de raisonnement |
| L'apparition plus ou moins rapide et intense des mécanismes protecteurs dépend pour beaucoup du polymorphisme de l'immunité d'un individu à l'autre, ce qui rend compte de la plus ou moins grande sensibilité individuelle aux infections/parasitoses : - en particulier, le polymorphisme du CMH influence l'aptitude à bien présenter et reconnaitre les antigènes impliqués dans la protection (cf immun2-02). - un autre élément du polymorphisme est le ratio Th1/Th2 (régulation de l'immunité humorale/cellulaire cf immun2-04) et l'activité du complément (cf immun1-13). |
| Plus les µorganismes/parasites sont complexes, et plus on assiste à des situations d'équilibre entre l'hôte et l'agent infectieux, avec l'acquisition progressive d'une immunité qui n'est que partiellement efficace (infections chroniques, infections latentes et portage asymptomatique..). Ceci explique par exemple la récurrence des accès herpétiques ("boutons de fièvre": rechute en cas de baisse de l'immunité) et des crises de paludisme (variant parasitaire échappant à la réponse immune). L'immunité contrôle alors le taux de replication pour maintenir une charge infectieuse faible, occasionnant peu de symptômes, mais ne parvient pas à éliminer complètement l'infection. |
| Les surinfections bactériennes (=infections secondaires) sont des éléments fréquents de complication des infections virales: - dans le cas d'infections par des virus provoquant une immunodépression (parvovirus des carnivores, retrovirus félins..) - dans le cas d'infections par des virus capables de détruire les épitheliums (muqueuses respiratoires ou digestives) Les bactéries en cause sont fréquemment des bactéries opportunistes, dont l'animal est déjà un "porteur sain" au moment de l'infection virale (pasteurellaceae, mycoplasmes, staphylocoques-streptocoques, entérobactéries, corynebactéries..). |
| Le stress peut réduire considérablement la qualité de la réponse immune, et de ce fait faciliter et aggraver les infections et les parasitoses. Le stress est une réaction endocrine générale d'un organisme qui lutte sans succès contre une agression organique (traumatisme..) ou psychologique (conflits hiérarchiques..). Les principales hormones produites lors de stress chronique sont des gucocorticoïdes produits par les surrenales: ces GC réduisent les capacités d'activation et de différenciation des cellules imùmunocompétentes, et diminuent la prolifération lymphocytaire. |
exemples de la physiopathologie et du diagnostic de différentes infections: leucose féline (FeLV: Feline Leucosis Virus), immunodéficience féline (FIV: Feline Immunodeficiency Virus), parvovirose canine, rage, brucellose bovine, tuberculose bovine : cf cours 3-04 |
références et cours disponibles |
pour en savoir plus:
- classification simplifiée des bactéries, virus et parasites d'importance vétérinaire (sur le site de l'ENVL)
- endotoxines et super-antigènes: cours de bactériologie médicale
- choc septique: http://www.infirmiers.com/etud/cours/urgrea/chocseptique.php
- "Host-microbe interaction: bacteria" Current Opinion in Microbiology, 2006, 9/1 p1-4, Chihiro Sasakawa and Jörg Hacker
page réalisée par le Dr Delphine Grézel, VetAgro Sup, Campus Vétérinaire de Lyon, le 2/12/11 . Merci pour les corrections, commentaires et suggestions ( delphine.grezel@vetagro-sup.fr)