 2
2 3
3 4
4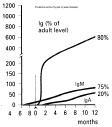
| accueil | immun 1-18: Immunité du jeune individu; transfert passif de l'immunité |
<-- cours --> |
objectifs pédagogiques (*) |
|
|
- décrire les étapes de l'acquisition de l'immunité humorale et cellulaire par le foetus et par le nouveau-né | |
définitions générales - messages |
|
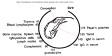
| immunité du foetus | La mise en place des organes et des cellules de l'immunité s'effectue progressivement au cours du développement foetal, suivant un schéma assez semblable chez tous les mammifères (fig1: étapes du développement de l'immunité chez le foetus). C'est le placenta et l'utérus qui assurent le rôle de barrière pour protéger le foetus contre les infections (et qui empêchent le foetus de subir les phénomènes de rejet d'un organisme histo-incompatible). De ce fait: - les capacités de défense du foetus contre les infections sont faibles, d'où un risque important de mortalité et d'avortement lors d'infection d'une femelle gestante (même par des germes non ou faiblement pathogènes pour un individu adulte). - le foetus ne possède pas ou très peu de capacité de rejet de greffes (d'où un grand nombre de modèles expérimentaux d'induction de tolérance et d'étude de greffes). - l'activité thymique (production et éducation des lymphocytes T) est maximale chez le foetus en fin de gestation et les lymphocytes produits vont coloniser tous les tissus et organes lymphoïdes secondaires. Le thymus involue au moment de la maturité sexuelle et est difficilement identifiable chez l'adulte (diminution du cortex et de la medulla), mais il faut noter toutefois que l'activité thymique persiste dans les tissus thymiques restants, tout au long de la vie de l'individu pour assurer le renouvellement du répertoire lymphocytaire (fig2: involution thymique et activité thymique du foetus, du jeune et de l'adulte). L'administration d'un antigène à un foetus in utero, en milieu de gestation, si elle n'a pas de conséquence toxique, peut conduire à un mécanisme de tolérance vis-à-vis de cet antigène (d'où le phénomène d'infection persistante immunotolérée= IPI). |
| immunité du jeune | Le nouveau-né est issu d'un utérus quasi-stérile, et il est "bombardé" d'antigènes de toutes natures dès sa naissance. Il possède une immunité particulière, dont les conséquences en matière d'immunité anti-infectieuse et anti-parasitaire sont très importantes: - l'immunité non spécifique et les principaux mécanismes d'immunité cellulaire (CTL, NK..) sont efficaces dès la naissance. L'immunité cellulaire est globalement similaire à celle de l'adulte à partir du 10ème jour. - l'immunité humorale se met en place lentement et on n'observe que très peu de réponse anticorps de type secondaire (en raison des délais nécessaires aux phénomènes de présentation des antigènes et de coopération). Le nouveau-né peut produire des anticorps de classe IgM, mais il n'est pas capable de produire une réponse anticorps efficace de classe IgG avant 3-4 semaines. Le taux d'IgG sériques atteint un taux proche de l'adulte seulement autour de 6-8 semaines, tandis que les IgA et les IgE apparaissent plus tardivement. La réponse IgA dans les muqueuses met plusieurs mois à atteindre le taux adulte (d'où une plus grande sensibilité du jeune aux infections ORL, respiratoires et digestives). - l'handicap immun du jeune en matière d'immunité humorale est compensé au cours des premières semaines de sa vie par le transfert passif d'anticorps entre la mère et le jeune: les IgG sériques chez le jeune sont la résultante d'un apport maternel précoce (via le placenta et/ou le colostrum) et de sa production propre (croissante). (fig3: transfert des Ig d'origine maternelle et taux d'Ig du jeune et fig4: production propre d'Ig de différentes classes par le jeune). - le jeune acquiert dès la naissance sa flore commensale cutanée et muqueuse au contact de la mère (et de l'environnement) (cf cours de bactériologie). Cette flore assure un rôle direct de barrière vis-à-vis des agents infectieux et contribue au développement de l'immunité anti-infectieuse. |
| transfert passif d'immunité maternelle | L'immunité humorale transférée par la mère: - est immédiate: le jeune est protégé par les anticorps transmis sans qu'un délai de réponse immune soit nécessaire - est passive: les Ig transférées par des mécanismes de transcytose à travers les barrières épithéliales reproduisent à l'identique les spécificités des anticorps maternels (un jeune issu d'une mère séropositive vis-à-vis d'un antigène X est également séropositif). - est temporaire: les anticorps maternels sont progressivement éliminés selon les modalités classiques de catabolisme des Ig (demi-vie des IgG: environ 3 semaines): l'immunité d'origine maternelle dure généralement moins de 12 semaines. - est limitée aux anticorps de classes IgG (IgG1 et IgG2) et IgA. Des variations spécifiques importantes modulent la classe et la voie de transfert (placenta, colostrum, lait). - est limitée aux spécificités antigéniques rencontrées par la mère dans les semaines précédant la naissance: le jeune est ainsi protégé contre les principaux µorganismes et parasites de l'environnement maternel. |
| Le transfert de l'immunité maternelle s'effectue par transcytose des Ig au travers des cellules epithéliales, grâce à l'expression de récepteurs spécifiques pour les IgG1 et les IgA. On observe plusieurs types de transfert, en proportion variable selon les espèces (cf tableau: passage placentaire et colostral des Ig): - par le placenta en fin de gestation (primates +++, rongeurs et lagomorphes++, carnivores et porcins +): le transfert des IgG via les récepteurs placentaires procure au jeune un taux d'IgG sérique significatif en fin de gestation. - par le colostrum (toutes espèces): le colostrum est une sécrétion mammaire particulière au cours des premiers jours suivant la mise-bas (maximum 10jours), qui contient un taux d'IgG très supérieur au sang, ainsi que des IgAs. Les IgG du colostrum traversent activement l'épithélium digestif jusque dans les tissus et le sang, tandis que les IgAs restent dans le tube digestif et procurent une immunité locale. - par le lait (toutes espèces): les IgAs et IgG produites par la muqueuse mammaire se retrouvent dans le lait à des quantités faibles et constantes durant toute la lactation. Il est très important de noter que le passage dans la circulation sanguine des IgG ingérées est un phénomène bref, qui a lieu dans les 0-24h suivant la naissance (ensuite les récepteurs epithéliaux pour les IgG ne sont plus exprimés, et il n'y a quasi plus de passage sanguin des IgG après 48h). Les Ig ingérées à partir du lait n'ont donc qu'un rôle de protection locale du tube digestif. |
|
| déficit de transfert passif maternel | Différents problèmes peuvent occasionner un déficit du transfert passif de l'immunité maternelle par la voie colostrale (ce déficit affecte surtout les équidés et les ruminants): - quantité d'IgG dans le colostrum insuffisante (souvent si la mise-bas survient plus tôt que la date prévue) - absence ou insuffisance de têtée dans les 24 premières heures (le plus souvent en raison d'un nouveau-né trop faible, mais également pour d'autres raisons comme le refus de la mère de se laisser têter..). L'hypogammaglobulinémie du jeune, lorsque le transfert maternel est insuffisant, ocasionne une grande sensibilité aux infections néonatales. Le vétérinaire a un rôle de conseil important auprès de l'éleveur pour que celui-ci vérifie la bonne prise du colostrum et y aide au besoin. Il est possible de traiter le déficit par une administration d'IgG, soit par voie orale (avant 48h), soit par injection (après 48h). |
schémas et figures |
|
tableaux |
références et cours disponibles |
Sur le serveur de l'ENVL:
pour en savoir plus :
- "Veterinary Immunology- an introduction 4th edition" I.Tizard, 1992, ed Saunders
- "Postnatal development of leukocyte subset composition and activity in dogs" M.Toman et al, Vet.Immunol.Immunopathol, 2002 (87/3-4, p321-326)
page réalisée par le Dr Delphine Grézel, VetAgro Sup, Campus Vétérinaire de Lyon, le 2/12/11 . Merci pour les corrections, commentaires et suggestions ( delphine.grezel@vetagro-sup.fr)